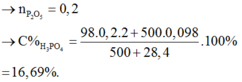Những câu hỏi liên quan
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là A. 17,04% B. 17,64% C. 16,69% D. 18,02%
Đọc tiếp
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là A. 17,04% B. 17,64% C. 16,69% D. 18,02%
Đọc tiếp
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Đáp án C
→ n P 2 O 6 = 0 , 2 → C % H 3 P O 4 = 98 . 0 , 2 . 2 + 500 . 0 , 098 500 + 28 , 4 . 100 % = 16 , 69 %
Đúng 0
Bình luận (0)
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là A. 17,04% B. 17,64% C. 16,69% D. 18,02%
Đọc tiếp
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Đáp án C.
→ n P 2 O 5 = 0 , 2 → C % H 3 P O 4 = 16 , 69 %
Đúng 0
Bình luận (0)
Hòa tan 28,4 gam photpho (V) oxit trong 500gam dung dịch axit photphoric có nồng độ 9,8%. C% của dung dịch axit photphoric thu được là: A. 17,04% B. 17,64% C. 16,69% D. 18,02%
Đọc tiếp
Hòa tan 28,4 gam photpho (V) oxit trong 500gam dung dịch axit photphoric có nồng độ 9,8%. C% của dung dịch axit photphoric thu được là:
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Hoà tan 14,2 gam điphotpho pentaoxit vào 180 gam nước.a) Tính khối lượng axit photphoric thu được.b) Tính nồng độ % của dung dịch axit photphoric.
\(n_{P_2O_5}=\dfrac{14.2}{142}=0.1\left(mol\right)\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(0.1..........................0.2\)
\(m_{H_3PO_4}=0.2\cdot98=19.6\left(g\right)\)
\(m_{dd}=14.2+180=194.2\left(g\right)\)
\(C\%H_3PO_4=\dfrac{19.6}{194.2}\cdot100\%=10.09\%\)
Đúng 2
Bình luận (0)
Hòa tan 14,2 gam P2O5 trong 250 g dung dịch H3PO4 9,8%. Nồng độ % của dung dịch axit H3PO4 thu được là:
A. 5,4
B. 14,7
C. 16,7
D. 17,6
Đáp án C
Ta có: nP2O5= 0,1 mol; mH3PO4 ban đầu= 250.9,8/100=24,5 gam
P2O5+ 3H2O→ 2H3PO4
0,1 0,2 mol
Tổng khối lượng H3PO4 là: 0,2.98+ 24,5=44,1 gam
Khối lượng dung dịch là: 14,2+ 250=264,2 gam
![]()
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 15,5 gam photpho bằng oxi dư rồi hoà tan sản phẩm vào 200 gam nước. Nồng độ phần trăm của dung dịch axit thu được là
Hòa tan 2,7 gam nhôm trong dung dịch axit sunfuric H2SO4 9,8% thu được V (lít) khí và dung dịch A.
a) Tính V (đktc)?
b) Tính khối lượng dung dịch H2SO4 9,8% cần dùng.
c) Tính nồng độ % dung dịch thu được sau phản ứng.
\(n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,15 0 ,05 0,15
a)\(V=0,15\cdot22,4=3,36\left(l\right)\)
b)\(m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,7}{9,8}\cdot100=150\left(g\right)\)
c) \(m_{H_2}=0,15\cdot2=0,3\left(g\right)\)
\(m_{ddsau}=2,7+150-0,3=152,4\left(g\right)\)
\(m_{Al_2\left(SO_4\right)_3}=0,05\cdot342=17,1\left(g\right)\)
\(\Rightarrow C\%=\dfrac{17,1}{152,4}\cdot100=11,22\%\)
Đúng 1
Bình luận (0)
1)Hòa tan hoàn toàn 9,6 gam sắt (III) oxit bằng dung dịch axit sunfuric 9,8% ta thu dung dịch A màu nâu đỏ.a. Tính khối lượng dung dịch axit cần dùng? b. Tính nồng độ phần trăm của dung dịch A thu được? C. Lấy toàn bộ dung dịch A tác dụng vừa đủ bằng dung dịch BaCl2 10,4%ta thu được một chất rắn màu trắngD. Tính khối lượng chất rắn D vàkhối lượng dung dịch BaCl2 cần dùng?
Đọc tiếp
1)Hòa tan hoàn toàn 9,6 gam sắt (III) oxit bằng dung dịch axit sunfuric 9,8% ta thu dung dịch A màu nâu đỏ.
a. Tính khối lượng dung dịch axit cần dùng?
b. Tính nồng độ phần trăm của dung dịch A thu được?
C. Lấy toàn bộ dung dịch A tác dụng vừa đủ bằng dung dịch BaCl2 10,4%
ta thu được một chất rắn màu trắng
D. Tính khối lượng chất rắn D vàkhối lượng dung dịch BaCl2 cần dùng?
Ta có: \(n_{Fe_2O_3}=\dfrac{9,6}{160}=0,06\left(mol\right)\)
a. PTHH: Fe2O3 + 3H2SO4 ---> Fe2(SO4)3 + 3H2O (1)
Theo PT(1): \(n_{H_2SO_4}=3.n_{Fe_2O_3}=3.0,06=0,18\left(mol\right)\)
=> \(m_{H_2SO_4}=0,18.98=17,64\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{17,64}{m_{dd_{H_2SO_4}}}.100\%=9,8\%\)
=> \(m_{dd_{H_2SO_4}}=180\left(g\right)\)
b. Ta có: \(m_{dd_{Fe_2\left(SO_4\right)_3}}=9,6+180=189,6\left(g\right)\)
Theo PT(1): \(n_{Fe_2\left(SO_4\right)_3}=n_{Fe_2O_3}=0,06\left(mol\right)\)
=> \(m_{Fe_2\left(SO_4\right)_3}=0,06.400=24\left(g\right)\)
=> \(C_{\%_{Fe_2\left(SO_4\right)_3}}=\dfrac{24}{189,6}.100\%=12,66\%\)
c. PTHH: Fe2(SO4)3 + 3BaCl2 ---> 3BaSO4↓ + 2FeCl3 (2)
Theo PT(2): \(n_{BaSO_4}=3.n_{Fe_2\left(SO_4\right)_3}=3.0,06=0,18\left(mol\right)\)
=> \(m_{BaSO_4}=0,18.233=41,94\left(g\right)\)
Theo PT(2): \(n_{BaCl_2}=n_{BaSO_4}=0,18\left(mol\right)\)
=> \(m_{BaCl_2}=0,18.208=37,44\left(g\right)\)
Ta có: \(C_{\%_{BaCl_2}}=\dfrac{37,44}{m_{dd_{BaCl_2}}}.100\%=10,4\%\)
=> \(m_{dd_{BaCl_2}}=360\left(g\right)\)
Đúng 0
Bình luận (0)